Eksperyment z serii płomień bez zapałek. Jeśli komuś w laboratorium skończą się zapałki bez problemu z kilku odczynników może wykrzesać płomień.
 W eksperymencie tym zastosowany zostanie silnie żrący, stężony kwas siarkowy !, Sama reakcja przebiegnie bardzo gwałtownie i istnieje możliwość wypryśnięcia silnie żrącej cieczy z naczynia.
W eksperymencie tym zastosowany zostanie silnie żrący, stężony kwas siarkowy !, Sama reakcja przebiegnie bardzo gwałtownie i istnieje możliwość wypryśnięcia silnie żrącej cieczy z naczynia.
Z uwagi na powyższe należy bezwzględnie założyć okulary ochronne i fartuch. Pamiętaj że jeśli zdecydujesz się wykonać ten eksperyment - robisz to na własną odpowiedzialność.
Po przeprowadzeniu doświadczenia należy dokładnie posprzątać wszystkie pozostałości po reakcji. Mogą być one bardzo niebezpieczne ze względu na zawartość stężonego kwasu siarkowego, oraz możliwość zapalenia łatwozapalnych przedmiotów !!.
Co nam będzie potrzebne:
1. Nadmanganian potasu KMnO4,
2. Stężony kwas siarkowy H2SO4,
3. Alkohol etylowy C2H5OH (może być denaturat),
4. Mała parowniczka,
5. Bagietka lub gruby drut,
6. Zwitek waty.
7. Pipeta szklana.
8. Statyw.

Przygotowanie eksperymentu:
Parowniczkę ustawiamy w stabilnym statywie lub na trójnogu. Wsypujemy do niej pół małej łyżeczki nadmanganianu potasu i w międzyczasie na bagietkę lub kawałek drutu nawijamy zwitek waty i nasączamy denaturatem. Teraz do wsypanego wcześniej do parowniczki nadmanganianu potasu dodajemy parę kropel kwasu siarkowego.
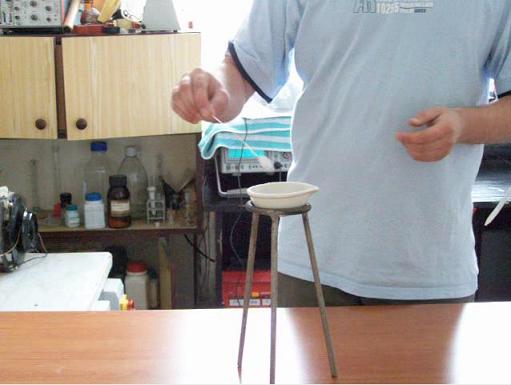
Teraz wystarczy tylko nasączonym zwitkiem waty dotknąć mieszaniny nadmanganianu potasu i kwasu. Natychmiast następuje gwałtowny zapłon alkoholu.
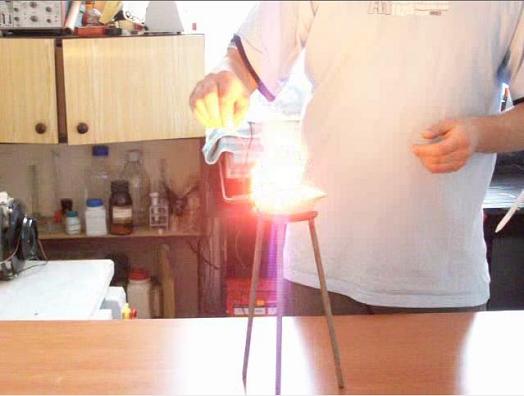
Zapalenie alkoholu jest tak gwałtowne, że może spowodować rozpryśnięcie nadmanganianu potasu. Eksperyment należy do bardziej niebezpiecznych, ale wykonany prawidłowo i z zachowaniem należytych środków ostrożności jest bardzo efektowny i bezpieczny.

Dlaczego alkohol się zapalił?
Podczas reakcji manganianu (VII) potasu z kwasem siarkowym(VI) powstaje tlenek manganu (VII), który rozkłada się z wydzielaniem tlenu. Powstający tlen gwałtownie utlenia alkohol etylowy, co obserwujemy w postaci gwałtownego rozbłysku.
2KMnO4 + H2SO4 => K2SO4 + Mn2O7 + H2O
2Mn2O7 => 4MnO2 + 3O2














